Les ciments d’aluminate de calcium (CAC), une réponse à la corrosion biogénique des bétons
Pourquoi les ciments aluminates de calcium ? Une innovation avec une longue histoire…
Le ciment d’aluminate de calcium (CAC) a été breveté en 1908 par Jules Bied, Directeur de la Recherche Lafarge, alors qu’il cherchait un ciment offrant une meilleure résistance aux sulfates que le ciment Portland ordinaire. Commercialisé dès la fin de la première guerre mondiale, il devint rapidement évident que le ciment alumineux présentait plusieurs autres propriétés très utiles. Le premier cas documenté rapportant la bonne tenue du ciment alumineux dans un réseau d’assainissement remonte à 1928, aux Pays-Bas. Au cours des décennies, les CAC ont été utilisés à travers le monde pour allonger la durée de vie des infrastructures d’assainissement, s’appuyant sur des observations terrains pragmatiques montrant une bien meilleure performance dans les réseaux d’assainissement.
Du point de vue normatif
Le ciment CAC est couvert par la norme européenne NF EN 14647 - Ciment d'aluminates de calcium — Composition, spécifications et critères de conformité (décembre 2006).
La formulation de bétons de ciment d’aluminate de calcium est encadrée par la norme NF EN 206+A2/CN (octobre 2022) qui précise au § NA.5.3.2.3 : « Dans le cas d’utilisation de ciments d’aluminates de calcium, en complément des exigences de NA.5.3.2.1, il convient d’appliquer la norme NF EN 14647, y compris son Annexe A et respecter en particulier la valeur maximale du rapport eau/ciment, le dosage minimal en ciment et les spécifications complémentaires relatives à la propreté des granulats et à la teneur en alcalins indiqués dans ces documents. »
Le mécanisme de la corrosion biogénique… ou comment de minuscules bactéries peuvent détruire un ouvrage
La corrosion biogénique dépend de l’activité biologique de différentes souches de bactéries acidophiles. Un minuscule film de bactéries Acidithiobacillus thiooxidans – parfois appelées Thiobacillus Concretivorus parce qu’elles « mangent » le béton – peut produire suffisamment d’acide sulfurique pour corroder jusqu’à 25 mm de béton par an lorsque les conditions les plus sévères sont réunies.
Pour choisir la bonne solution à ce problème, il est essentiel de comprendre le mécanisme de corrosion biogénique.
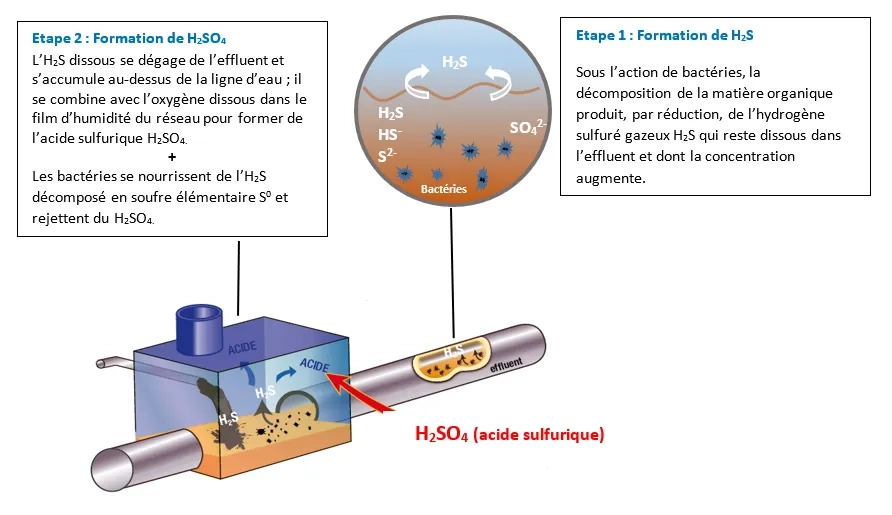
Le ciment d’aluminates de calcium (CAC), une solution pour protéger les bétons soumis à la corrosion biogénique
Les bétons formulés à base de ciment d’aluminates de calcium bénéficient des mécanismes de protection suivants :
Lorsque les bactéries colonisent une surface neuve d’un mortier d’aluminates de calcium, la première attaque de l’acide sulfurique produit une réaction de neutralisation avec les phases aluminates de calcium.
Les hydrates d’aluminates de calcium (Ca + Al + H2O) sont dissous et réagissent avec H2SO4 pour précipiter à la fois en sulfate de calcium (CaSO4 .2H2O) et en alumine hydratée (AH3). Tel qu’illustré par la Figure 1, la capacité de neutralisation basique par unité de poids de l’aluminate de calcium est d’environ 40 % supérieure à celle du ciment Portland pour un faible pH.
Autrement dit, il faut plus d’acide pour dissoudre la même quantité de CAC.
Il est à noter que certains mortiers peuvent être composés à 100 % d’aluminates de calcium, donc la totalité du produit réagit, et pas seulement la fraction de liant.

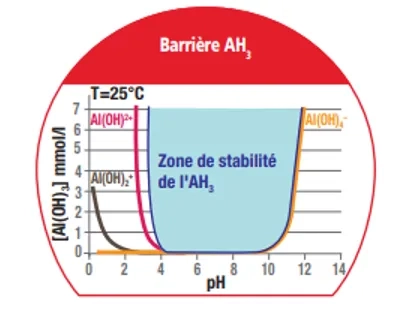
Le résultat de la première attaque acide est la précipitation d’une couche amorphe dense d’alumine hydratée AH3 à la surface. Cette couche d’alumine hydratée est très importante car elle est chimiquement stable jusqu’à un pH aussi faible que 3-4. Ainsi, la précipitation de l’AH3 crée une véritable barrière physique de quelques centaines de microns d’épaisseur qui s’oppose à la pénétration de l’acide sulfurique tant que le pH demeure supérieur à 3-4. Cette barrière constitue la seconde ligne de défense des aluminates de calcium. (Figure 2)
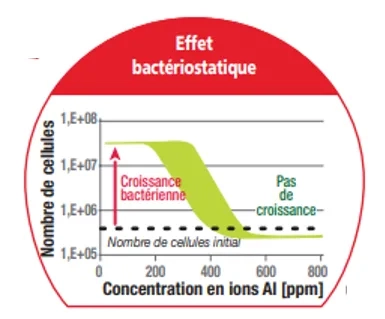
Lorsque l’action continue des bactéries a produit suffisamment d’acide sulfurique pour abaisser le pH sous le seuil de solubilité de l’alumine hydratée, l’AH3 se dissous et libère des ions aluminium dans le biofilm qui adhère à la surface. Parce que le biofilm est très mince, la concentration locale en ions aluminium augmente rapidement. La présence d’alumine libre produit rapidement un « effet bactériostatique », qui se traduit par une réduction radicale de l’activité des bactéries. L’activité bactérienne est affectée de telle sorte que la production d’acide est drastiquement réduite, voire stoppée. (Figure 3)

En conclusion
La conséquence essentielle de l’effet bactériostatique activé par les aluminates de calcium est que le pH de surface se stabilise autour du seuil de solubilité de l’alumine, autour de pH 3-4.
Cela implique que lorsque la barrière d’alumine hydratée s’est formée, elle va protéger très durablement la structure. Le cycle de l’alumine reste alimenté par les réserves d’aluminate de calcium sous la couche d’AH3. Même si une partie de l’alumine doit être dissoute avec le temps pour maintenir les conditions bactériostatiques, la concentration en acide demeure 100 à 1000 fois plus faible que les surfaces de réseaux où l’on mesure un pH de 1. Un pH plus élevé implique des conditions bien moins agressives et donc une bien plus longue durée de vie de la barrière d’alumine hydratée.
-
Documentation technique
-
La Teste-de-buche
-

COMMENTAIRES
LAISSER UN COMMENTAIRE